לאחר שאחיו מת לנגד עיניו מסרטן ששום תרופה לא ריפאה, אחד מחוקרי הסרטן הידועים בעולם קורא לאסטרטגיה חדשה לטיפול במחלה
X זמן קריאה משוער: רבע שעה
התשובות שברט ווגלסטין היה זקוק להן, התשובות שחשש מהן, נמצאו בדגימת הדם. ווגלסטין הוא אחד המדענים המצוטטים ביותר בעולם. בשנות ה-80 הוא תואר כמי שהצליח לפרוץ ל"תא הטייס של הסרטן" אחרי שהוא ועמיתיו באוניברסיטת ג'ונס הופקינס הראו לראשונה בדיוק כיצד סדרה של מוטציות דנ"א, המצטברות בשקט לאורך עשרות שנים, הופכות תאים לסרטניים. הוא עזר להוכיח שדנ"א שניזוק הוא הגורם לסרטן. וכעת דמיינו לכם שתוכלו לראות את המוטציות האלה – את הסרטן עצמו – במבחנה של דם. כמעט כל סוגי הסרטן משירים דנ"א בדם, והמעבדה של ווגלסטין בג'ונס הופקינס פיתחה טכניקה שנקראת "ביופסיה נוזלית" ומזהה את החומר הגנטי הזה.

ברט ווגלסטין. צילום: אתר אוניברסיטת ג׳ון הופקינס
הטכנולוגיה הזו התאפשרה בעזרת כלים שמרצפים במהירות את הדנ"א שבדגימת דם, כך שחוקרים יכולים לזהות דנ"א של גידול גם כשנותרו ממנו כמויות מזעריות בלבד. המדענים מג'ונס הופקינס, בעזרת רופאים מהמרכז האונקולוגי הגדול ביותר בבולטימור, חקרו את דמם של יותר מ-1,000 מטופלים. הם אומרים שביופסיות נוזליות מזהות סרטן עוד לפני שתסמיני המחלה מופיעים.
אבל דגימת הדם הספציפית הזו היא עניין אישי. היא שייכת לאחיו של ווגלסטין, מנתח אורטופדי הצעיר ממנו בשנה. הוא נאבק בסרטן העור, והמחלה כבר החלה להתפשט. הייתה תקווה שמצבו ישתפר בעזרת תרופה חדשה, אבל הטיפול גורם לנפיחות, וקשה לומר לפי סריקות הרנטגן וה-CT אם הסרטן נסוג או לא. אז ווגלסטין השתמש בטכנולוגיה החדשה מהמעבדה שלו. אם הדנ"א הסרטני נעלם מהדם, הם יחגגו. אם הוא עדיין שם, אולי הוא יוכל להפנות את אחיו לאיזושהי תרופה אחרת בניסיון נואש אחרון. "ניסינו לכוון את הטיפול. זה מה שרצינו לעשות, בכל אופן," אומר ווגלסטין. הוא משתנק. הוא לא מספר מה קרה אחר כך.
מודעת האבל של בארי ווגלסטין, יליד בולטימור, הופיעה ב-3 ביולי, 2013.
אנחנו לא מנצחים במלחמה נגד הסרטן, ומותו של בארי ווגלסטין מראה למה. יותר מדי מקרי סרטן מאובחנים רק כשכבר אי אפשר לרפא אותם. מדי שנה מושקעים ברחבי העולם 91 מיליארד דולר בטיפול בסרטן, אבל רוב הטיפולים האלה מוגשים לחולים בשלב מאוחר מדי. הטיפולים החדשים ביותר, שפותחו בהוצאה כספית אדירה, עולים 10,000 דולר לחודש ולרוב מאריכים את חיי המטופל בכמה שבועות בלבד. חברות התרופות מפתחות ובודקות יותר תרופות לסרטן מתקדם מאשר לכל מחלה אחרת.
יותר מדי מקרי סרטן מאובחנים רק כשכבר אי אפשר לרפא אותם. מדי שנה מושקעים ברחבי העולם 91 מיליארד דולר בטיפול בסרטן, אבל רוב הטיפולים האלה מוגשים לחולים בשלב מאוחר מדי
"אנחנו, הציבור והמדענים, שבויים ברצון לרפא סרטן בשלב מתקדם," אומר ווגלסטין. "זאת האסטרטגיה המקורית של החברה. אני לא חושב שזה מחויב המציאות." יש דרכים נוספות להפחית את מקרי המוות מסרטן: להשתמש בקרם הגנה, להימנע מעישון ולהיבדק כדי לתפוס את המחלה בשלב מוקדם. מבחינת ווגלסטין, כל הצעדים המונעים האלה הם חלק מהאסטרטגיה החלופית, שזוכה להרבה פחות תשומת לב ומימון. אבל כשהמניעה עובדת, היא מניבה תוצאות טובות יותר מכל תרופה. בארצות הברית, הסיכוי למות מסרטן המעי הגס נמוך ב-40 אחוז משהיה ב-1975, ולירידה הזאת אחראית בעיקר בדיקת הקולונוסקופיה. גם במלנומה אפשר לטפל בעזרת ניתוח אם תופסים אותה מוקדם. "אנחנו חושבים שהאסטרטגיה החלופית צריכה להיות דרך הפעולה העיקרית," אומר ווגלסטין.
יכול להיות שבדיקות הדם החדשות יאפשרו זאת. החוקרים מג'ונס הופקינס אומרים שהם מתקרבים לראשונה ליצירת כלי בדיקה כללי שיבצע סריקה רחבה – אולי במסגרת בדיקה פיזית שנתית – לאיתור עקבות מולקולריות של סרטן באנשים שלא סובלים מתסמיני המחלה. "אנחנו חושבים שפתרנו את בעיית האבחון הראשוני," אומר ויקטור ולקולסקו, חוקר מג'ונס הופקינס שמנהל מעבדה בבניין הסמוך לזה של ווגלסטין. יהיה קשה להפוך את הבדיקות האלה לכלי שגרתי ברפואה. למשל, בעוד שהבדיקה תוכל לזהות דנ"א סרטני בגוף, הרופאים לא יידעו איפה הגידול נמצא, עד כמה הוא מסוכן, ואפילו אם הוא מצדיק טיפול. "אנחנו צריכים להיות זהירים בעניין הזה," אומר דניאל הייבּר, מנהל מרכז הסרטן בבית החולים מסצ'וסטס ג'נרל. הוא חושב שבדיקות הדנ"א בדם "אינן מוכנות לשימוש" ואומר שיידרשו מחקרים גדולים מאוד כדי להוכיח את יעילותן. "יש משוכה גבוהה לעבור," הוא אומר.
למרות הספקנות, הטכנולוגיה זוכה לתשומת לב רבה. טוני דיקהרבר, ראש תוכנית טכנולוגיות הניתוח המולקולרי החדשניות במרכז הלאומי לסרטן, אומר שרק לפני שלוש שנים, חיפוש דנ"א סרטני בדם נחשב במקרה הטוב לרעיון מהשוליים הרפואיים. אבל כעת מעבדות וחברות מקליפורניה ולונדון עולות על הגל ומתחילות לייצר שיפורים רבים לטכנולוגיית בדיקת הדם ולהזרים נתונים חדשים המעידים על יעילותה. "אנשים מתחילים לחשוב ש[ווגלסטין] צודק – שזאת אולי הדרך הטובה ביותר לאבחון מוקדם," הוא אומר. "יהיה אפשר ליישם [אותה] בצורה נרחבת יותר מטכנולוגיות אחרות שאנו משתמשים בהן, ונוכל לזהות מגוון עצום של סוגי סרטן."
נכון לעכשיו נראה שאם הבדיקה מוצאת אצלכם דנ"א של גידול, אתם אכן חולים בסרטן. וייתכן שזה היתרון של בדיקה זו על פני הבדיקות הנוכחיות של סרטן הערמונית וסרטן השד, שמניבות מקרים רבים של "חיובי-כוזב"
בפברואר הגישו רופאים מג'ונס הופקינס ו-23 מוסדות אחרים את הסקירה הגדולה ביותר עד כה של ממצאיהם. הם חקרו גידולים של 846 מטופלים עם 15 סוגים שונים של סרטן. הם מצאו דנ"א של גידולים בדמם של יותר מ-80 אחוז מהמטופלים הסובלים מסרטן מתקדם שהספיק להתפשט, ובדמם של כ-47 אחוז מהמטופלים הסובלים מסרטן מקומי הנמצא בשלב המוקדם ביותר. והם הצליחו לזהות את הדנ"א בכל המקרים המתקדמים של סרטן המעי הגס. התוצאות לא נראות מרשימות בתחילה. בדיקה שמפספסת חצי מהמקרים? התועלת היא שהבדיקות "ספציפיות להפליא," אומר ולקולסקו.
נכון לעכשיו נראה שאם הבדיקה מוצאת אצלכם דנ"א של גידול, אתם אכן חולים בסרטן. וייתכן שזה היתרון של בדיקה זו על פני הבדיקות הנוכחיות של סרטן הערמונית וסרטן השד, שמניבות מקרים רבים של "חיובי-כוזב". "זה נורמלי ששאריות דנ"א נמצאות בדם; זה נורמלי ששאריות הדנ"א תואמות גידולים," אומרת סטפני ג'פרי, מנהלת חקר האונקולוגיה הכירורגית באוניברסיטת סטנפורד. מבחינת ווגלסטין, משמעות בדיקות הדם האלה היא שאולי נוכל לתפוס יותר ממחצית ממקרי הסרטן בשלב מוקדם, ואף לרפאם בניתוח. "לו הייתה מתגלה תרופה שמרפאת חצי ממקרי הסרטן היו עושים פסטיבל באמצע ניו יורק," הוא אומר.
המלחמה בסרטן
הנשיא ניקסון השיק את המלחמה בסרטן ב-1971, כשווגלסטין עוד היה סטודנט לרפואה. ואז באו שנים של תסכול מכיוון שהתרופות לא הצליחו להפחית בצורה משמעותית את מספר מקרי המוות מסרטן. אבל כעת אנחנו יודעים מה גורם לסרטן. עבודתו של ווגלסטין בשנות ה-80, שאותה עשה עם עמיתו קנת קינזלר, עזרה בהמחשת תפקידן המהותי של מוטציות גנטיות במחלה. ומדענים כבר יצרו רשימה של 150 גנים שנראים כגורמים מרכזיים לסרטן. אף על פי שהנוף הגנטי של הסרטן הוא מורכב, כל מוטציות הדנ"א עושות דבר אחד: הן מאפשרות לתאים מסוימים להמשיך להתחלק במצבים שבהם תאים נורמליים מתים. חוסר האיזון הנובע מכך הוא סרטן.
אף על פי שהנוף הגנטי של הסרטן הוא מורכב, כל מוטציות הדנ"א עושות דבר אחד: הן מאפשרות לתאים מסוימים להמשיך להתחלק במצבים שבהם תאים נורמליים מתים
מבחינת חברות התרופות, התובנה הזאת ורשימת הגנים היוו נקודת זינוק למאמצים יקרים מאוד לפיתוח תרופות חדשות לסרטן מתקדם. אבל מבחינת ווגלסטין, לידיעה שמוטציות דנ"א הן הגורם לסרטן תמיד הייתה משמעות שונה: שאפשר לזהות את השינויים המעידים על סרטן כבר בשלב מוקדם, זמן רב לפני שהמחלה מאובחנת בדרך כלל. ובאונקולוגיה יש אמת מוסכמת: ככל שמזהים סרטן מוקדם יותר, כך סיכויי ההישרדות טובים יותר.
הנה לדוגמה את סרטן המעי הגס, שאותו חקר ווגלסטין בצורה המקיפה ביותר. הוא מתחיל במוטציה בודדה בגן שנקרא APC. אבל מנקודה זו עוברות בממוצע 30 שנים עד שהתאים רוכשים כמה מוטציות דנ"א נוספות שהן צריכות כדי להתפשט ולהרוג. כ-600,000 איש מתים מדי שנה מסרטן המעי הגס. "כמעט כולם ימותו רק מפני שהסרטן לא אובחן ב-27 השנים הראשונות לקיומו של הגידול," אומר ווגלסטין. "זה חלון זמן עצום שבמהלכו אפשר להתערב בתהליך."
הבעיה היא שעד בדיקות הדם החדשות, לא הייתה דרך פשוטה לחפש את המוטציות האלה. ווגלסטין עובד על תוכניות לאבחון מוקדם מאז שנות ה-90, כשהתחיל לחפש דנ"א של גידולים בשתן ובצואה בעזרת השיטות המייגעות שהיו זמינות אז. הוא מאמין שמניעה ובדיקה עדיין זוכות לתשומת לב מעטה מדי, ובמובן זה הוא "מיעוט מוחלט" בקרב החוקרים גם כיום. הוא מעריך שההשקעה הכספית במחקר של תרופות גדולה פי 100 מההשקעה בחקר האסטרטגיות האלה.
ואולי זה מסביר מדוע ווגלסטין ממורמר, למרות המוניטין שלו. קבוצת המחקר מג'ונס הופקינס, שכוללת כמה חוקרים ידועים נוספים, ממהרת לפרסם רעיונות חדשים, אבל מנסה גם לעתים קרובות ליירט קונספטים מדעיים שצברו פופולריות במקומות אחרים. כל מדען צעיר שרוצה לעבוד שם צריך, לפי המסורת של המעבדה, להציג תחילה את עבודתו המדעית הקודמת כשלראשו כתר של "ברגר קינג".
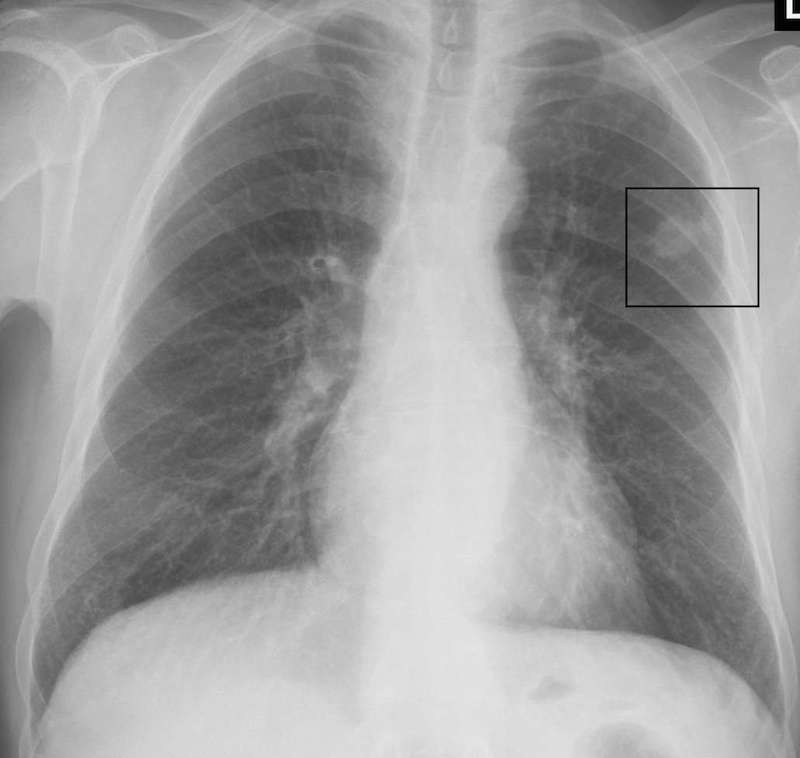
צילום רנטגן של גידול סרטני בריאות, כפי שמסומן מימין.
את עבודת המעבדה על בדיקות הדם מוביל לואיס דיאז, אונקולוג שהפך לבן חסותו של ווגלסטין. הוא עלה על הרעיון של חיפוש דנ"א סרטני בדם ב-2005, בזמן שחקר את האפשרות להשתמש בחיידק טורף כדי לחסל גידולים. עבודה זו כללה השתלת סרטנים אנושיים בעכברים, ודיאז נזכר שהוא "היה זקוק לשיטה לנטר את הגידול בעכבר בלי להרוג אותו." הוא ואחד מעמיתיו החליטו שאולי הם יהיו יכולים לעשות זאת בעזרת בדיקת דם. במהרה הם ראו שרמת הדנ"א האנושי עולה ויורדת בהתאם למידת ההצלחה, או חוסר ההצלחה, של הטיפול. אם הם יכולים לנטר דנ"א מגידול אנושי בעכברים, הם יוכלו לנטר אותו גם בבני אדם, לא?
זה לא היה רעיון חדש לגמרי. מאז 1948 ידוע שדנ"א צף לו בחופשיות בוורידים ובעורקים. לרוב מדובר בפסולת של תאים מתים. אבל גם גידולים משאירים דנ"א בדם. שיעור הדנ"א בדם שמגיע מגידולים עלול להגיע ל-87 אחוז באדם הגוסס מסרטן, אבל לעתים קרובות מדובר בכמות זעירה. כשדיאז החל לבחון את הנושא, הנתונים האלה עדיין לא נחשבו לעובדות, אלא לאפשרות מעורפלת. כדי לפתח את הביופסיה הנוזלית נדרשו החוקרים מג'ונס הופקינס להמציא תחילה דרכים לדלות דנ"א של גידול מתוך כמות עצומה של דנ"א נורמלי. החוקרים קיבלו דגימות דם ממטופלים של דיאז בבולטימור, אנשים החולים בסרטן המעי הגס. בתחילה הם חיפשו רק ארבעה גנים של סרטן. אבל הם ראו שהדנ"א של הגידול נעלם במהירות מהדם – תוך יום אחד במקרים מסוימים – אחרי שהמטופלים עוברים ניתוח או טיפול תרופתי. אצל נבדקי הביקורת הבריאים מעולם לא זוהה דנ"א סרטני. "הבנו שהבדיקה מסוגלת לשאול את השאלה 'האם יש לי סרטן?'" אומר דיאז.
ווגלסטין מעריך שגידול צריך לכלול לפחות עשרה מיליון תאים – כלומר להיות בגודל של ראש סיכה – כדי להשיר כמויות דנ"א שאפשר לזהות. לעומת זאת, כדי שיהיה אפשר לזהות גידול ב-MRI, הוא צריך להיות גדול פי 100
בג'ונס הופקינס מאמינים שהבדיקה רגישה יותר מכל שאר הכלים הקיימים – לפחות בכל הנוגע למקרי סרטן קטנים שאי אפשר לראות במכונת דימות. ווגלסטין מעריך שגידול צריך לכלול לפחות עשרה מיליון תאים – כלומר להיות בגודל של ראש סיכה – כדי להשיר כמויות דנ"א שאפשר לזהות. לעומת זאת, כדי שיהיה אפשר לזהות גידול ב-MRI, הוא צריך להיות גדול פי 100 ולהכיל לפחות מיליארד תאים. צוות החוקרים החל להשתמש בבדיקות הדנ"א בניסיון לקבוע אם תאים ממאירים נותרים גם במטופלים שגידוליהם הוסרו בניתוח. בשיתוף עם פיטר גיבס, אונקולוג אוסטרלי, הם סרקו את דגימות הדם של 250 מטופלים שעברו ניתוח לטיפול בסרטן מעי בשלב מוקדם. התברר שרוב האנשים האלה נרפאו, אבל כ-30 אחוז צפויים לסבול מהישנות של המחלה מכיוון שלא כל תאי הגידול הוסרו. הבעיה היא שרופאים לא יודעים אילו מטופלים יידרדרו שוב. "המנתח יאמר, 'אל תדאג – הוצאנו הכול,'" אומר דיאז. "אותי זה מתסכל, כי אז אני צריך לומר למטופל, 'אנחנו לא באמת יודעים אם נרפאת.'" השורדים נתקעים במצב של אי-ודאות כי אינם יודעים אם המחלה תחזור, ואולי בצורה מסוכנת אף יותר. והמצב הזה עלול להיגרר שנים.
המטופלים האוסטרליים עוברים בדיקות לאיתור דנ"א סרטני בדמם שישה שבועות לאחר הניתוח. עד כה, אומרים החוקרים, הם זיהו נכונה כחצי מהאנשים שהידרדרו לאחר מכן. בעתיד, אומר ווגלסטין, יהיה אפשר לזהות את המטופלים האלה ולתת להם כימותרפיה, שתציל לפחות שליש מהם. אבל מגבלות הבדיקה ברורות, מכיוון שהיא מפספסת חצי מהחולים שהסרטן חוזר ותוקף בעתיד. דיאז אומר שייתכן כי הסיבה לכך היא שהתאים הסרטניים שנשארים לא מפיקים כמות דנ"א שאפשר לזהות. "יכול להיות שהגענו לתקרה ביולוגית," הוא אומר. עם זאת, הדנ"א הסרטני עלול לעלות עם הזמן לרמות הניתנות לאיתור, ובדיקות תקופתיות של המטופלים יוכלו לגלות זאת. אף על פי שהבדיקה של ג'ונס הופקינס היא עדיין בגדר ניסוי, דיאז אומר שהוא בטוח בה מספיק כדי לומר למטופלים מסוימים שהם עדיין חולים ולאחרים שהם ככל הנראה החלימו. "שישה עד שמונה שבועות אחר כך אנחנו יודעים לומר להם אם הם נרפאו," הוא אומר. "זה מספק מאוד."
בדיקה המונית
ווגלסטין אומר שמטרתו הסופית היא להפוך את בדיקות הדם האלה לבדיקת סרטן שגרתית בשביל כלל האוכלוסייה. החוקרים מג'ונס הופקינס מאמינים שהם הגיעו לגרסה של הבדיקה המתאימה לכך. במקום לנטר כמה גנים סרטניים מרכזיים, הם מרצפים את כל הגנום של האדם בעזרת דנ"א מדגימת הדם. כך הם יכולים לראות באיזו תדירות חתיכות של חומר גנטי מופיעות במקום לא מתאים או נראות משובשות. כמות גדולה של דנ"א "מאורגן מחדש" היא תופעת לוואי מולקולרית שמופיעה רק בכרומוזומים של תאים סרטניים – סימן מעיד לנוכחותו של סרטן. אבל ריצוף גנומי מלא הוא עדיין עסק יקר. "כשאדם חולה בסרטן לא אכפת לך להוציא 5,000 דולר על בדיקת דנ"א. אבל אי אפשר להכניס הליך של 1,000 דולר לבדיקה הגופנית השנתית," אומר ווגלסטין. "המטרה היא להוזיל את הטכנולוגיה מספיק כדי שיהיה אפשר להשתמש בה באופן שגרתי."
וייתכן שיעבור עוד זמן רב לפני שזה יקרה. עלות ריצוף הדנ"א יורדת במהירות, אבל יכול להיות שגנום במאה דולר – מחיר שעשוי להיות נמוך מספיק בשביל בדיקה שגרתית – יגיע רק עוד עשר שנים. בינתיים, בג'ונס הופקינס התחילו במחקרים, שנעשים רובם באנשים עם פרה דיספוזיציה לסרטן, כדי לקבוע אם הטכניקה הזו תוכל לזהות גידולים ראשוניים באנשים בריאים. אחד המחקרים כולל 800 אנשים בקבוצת סיכון לסרטן הלבלב. במקרים החריגים האלה ישנן ציסטות על הלבלב שלפעמים מתפתחות לסרטן ולפעמים לא. הניסוי הקליני החל לעקוב אחרי המטופלים ב-2012, והחוקרים יוכלו לבחון לראשונה את התוצאות בהמשך השנה.
סרטן הלבלב הוא מקרה מבחן טוב לאבחון מוקדם. הוא לא שכיח מאוד, ובכל זאת הוא הגורם הרביעי בחומרתו למוות מסרטן בארצות הברית כיוון שמצליחים לרפא אותו רק ארבעה אחוזים מהזמן. אם מזהים אותו בשלב מוקדם מאוד, לפני שהוא מתפשט, סיכויי ההישרדות עולים ל-25 אחוז (סטיב ג'ובס, מייסד אפל, מת מסוג אחר של סרטן הלבלב, שנקרא "גידול נוירואנדוקריני", בגיל 56).
אבל הרחבת בדיקות הדנ"א לכלל האוכלוסייה היא קפיצה אדירה. הייבר, האונקולוג ממסצ'וסטס ג'נרל, אומר שהטכנולוגיה, כפי שהיא כיום, עשויה לגלות לרופא אם יש סרטן. אבל בניגוד לסריקת דימות או ביופסיה, היא לא בהכרח תאמר לו איפה בגוף הוא נמצא. המטופלים יפחדו, הרופאים לא ידעו איך לפעול. "המחשבה שנצטרך לבדוק אנשים בריאים ולומר להם, 'שמע, יש סרטן איפשהו אבל אנחנו לא יודעים בדיוק איפה' – זה מה שיפיל את כל [הפרויקט]," אומר הייבר.
בתחום הרפואה כבר היו מקרים של טיפול לקוי בבדיקות חיזוי. לדוגמה, בדיקת ה-PSA, שמזהה חלבון הקשור לסרטן הערמונית. לא רק שהבדיקה מייצרת "חיוביים-כוזבים" רוב הזמן, אלא שחלק מהגידולים שהיא מזהה גדלים באטיות רבה כל כך עד שלא משתלם לטפל בהם. מיליוני גברים קיבלו טיפולים לסרטן שכלל לא עמד להשפיע עליהם. לפי אחת ההערכות, על כל 47 גברים שבלוטת הערמונית שלהם נכרתה נמנע רק מוות אחד מסרטן. מחקרים שערכו חוקרים מדרטמות' קולג' מראים כי ממוגרפיה מובילה לאבחון יתר וטיפול יתר. כ-25 אחוז ממקרי סרטן השד שמתגלים ומטופלים לא היו מייצרים שום תסמין. "בודקים את כולם ומטפלים באנשים בגלל מחלות שלעולם לא היו משפיעות עליהן, כי הן לא היו מתפתחות או כי אנשים מתים מדברים אחרים," אומר ג'ונתן סקינר, כלכלן בריאות מדרטמות'. "החיסרון הפוטנציאלי של בדיקה מוקדמת הוא גדול."
אבל בג'ונס הופקינס, ולקולסקו אומר שהוא מאמין כי בעתיד ייערכו בדיקות דנ"א כלליות לאבחון סרטן. "אם אתה לא יכול לשנות את המצב, אולי אתה מעדיף לא לדעת," הוא אומר. "אבל קשה לי להאמין שהידיעה על סרטן לא תעזור לחולה. אולי לא נגיב בדרמטיות לכל פיסת מידע. אולי לא נעשה שום דבר. אבל את הבדיקות האלה יהיה כל כך קל להמשיך לעשות, שנוכל לומר למטופל, 'בוא נראה איך זה מתפתח.'"
חברו התרופות עדיין לא מדברות בריש גלי על בדיקה נרחבת לסרטן במטופלים בריאים לכאורה. נכון לעכשיו, Personal Genome Diagnostics, חברת הזנק בתחום האבחון שהוקמה על-ידי דיאז וולקולסקו, כמו גם כמה מתחרות כמו Boreal Genomics ו- Guardant Health, מציעות ביופסיה נוזלית אך ורק למטופלים החולים בסרטן מתקדם מאוד. החולים האלה יוכלו ללמוד מהבדיקה אם הטיפול עובד, ולהחליט אם לנסות משהו אחר במידה שלא. שימוש יעיל נוסף בטכנולוגיה הוא ניטור מוטציות הדנ"א הספציפיות שגורמות לגידולים אצל המטופל. מכיוון שלא מעט מתרופות הסרטן החדשות הן "ממוקדות" – כלומר חוסמות תהליכים מולקולריים ספציפיים – המטופלים מקבלים אותן רק אם הגידול שלהם הוא מהסוג שצפוי להגיב להן. רופאים יכולים כבר עכשיו לערוך בדיקות דנ"א בחלקי גידול שנאספו בביופסיית רקמות. אבל בדיקות דם בלתי פולשניות יהיו קלות ובטוחות יותר, ויאפשרו למטופלים להיבדק לעתים תכופות יותר. מכיוון שדנ"א סרטני עובר מוטציה ללא הרף, בדיקות אלה יוכלו לעזור למטופלים לדעת מתי עליהם להחליף תרופות.
מבחינתו של חלמי א-טוח'י, מנכ"ל Guardant Health, ביופסיות נוזליות הן "רעיון אדיר" בעל יישומים רבים. מסיבות מסחריות ורפואיות, החברה שלו משווקת בינתיים את הבדיקות רק לחולי סרטן. אבל הוא אומר שבדיקות לאבחון מוקדם הן תחום שהחברה שלו מתכוונת לעסוק בו. "זה ללא ספק הגביע הקדוש," הוא אומר. "תארו לכם את היישומים, ועל זה אנחנו עובדים."
שאלתי גם את ווגלסטין, בן 65, וגם את ולקולסקו, 44, אם אי פעם נבדקו בעצמם. שניהם ענו שלא. אבל בסך הכול, לגברים אמריקאים יש סיכוי של 40 אחוז לחלות בסרטן במהלך חייהם, והסיכויים רק הולכים ועולים עם הגיל. אם החוקרים האלה לא רצו להיבדק בעצמם, ספק אם הציבור הרחב ירוץ לעשות זאת. כדי שבדיקה לאבחון סרטן תהפוך לכלי בריאותי שגרתי תצטרך כל הקהילה הרפואית להשתתף במאמץ, ולשם כך יידרש זמן רב. ווגלסטין לא תמים. בכל מקרה נזדקק לתרופות כדי לטפל באנשים שיחלו בסרטן למרות הכול. אבל הוא משוכנע שהדרך הטובה ביותר להביס את המחלה היא למנוע אותה. כשהבעתי את תנחומיי על מות אחיו הוא פטר אותם במחוות יד. "זאת הסיבה שאנחנו עובדים על זה," הוא אומר. "עוד מאה שנה סרטן ומוות מסרטן יהיו הרבה יותר נדירים, וזה יקרה בזכות אבחון מוקדם, ולא כי גילינו איך לרפא גוף מוכה גידולים."
אנטוניו רגלאדו הוא עורך העסקים של ה-MIT Technology Review.
© 2014 Technology Review, INC. Distributed by Tribune Media Services, Inc.
 מחשבות מתחילות כאן
מחשבות מתחילות כאן

תגובות פייסבוק
תגובה אחת על מעט מדי מאוחר מדי
הדרך שבה מתקדם המחקר הרפואי קשורה לטוב ולרע למבנה הכלכלי-חברתי שבתוכו היא מתקיימת. אם תקראו בעיון את הכתבה תגלו שכל אחד מדבר מתוך הפוזיציה שלו במבנה הזה, וטוען בלהט שרק הוא צודק ומי שטוען כנגדו טועה ומטעה מטפשות אם לא מאינטרס.
ולכן אין טעם בכל הדיון - הישגי המדע הם מה שהם הודות למבנה הכלכלי-חברתי וגם הכישלונות והעיכובים כך.
אין לצפות שיקום מבנה-כלכלי אוטופי שבו כל אחד יפעל ללא מניעים אנוכיים ויתרום את מרצו וכשרונו לטובת הכלל. רק במבנה אוטופי כזה לא תהיינה מלחמות חוקרים ולא יתקיימו מאבקי כח על תקציבים, חוקרים יודו בחפץ-לב שעמיתיהם הצליחו היכן שהם נכשלו ומחקרים יקבלו את המקום הראוי להם ולא את המקום שמערכת יחסי-ציבור השיגה עבורם.
אז זה מה שיש, ובתוך המרק הסמיך הזה יש לשחות ולהגיע.
אקראיות מחושבת היטב
ג'ורג' שפירומספרים אקראיים חיוניים למחקר, לטכנולוגיה ולבטחוננו. החיפוש אחריהם מתגלה כמורכב מאוד, וחושף...
X 8 דקות
קונצרט השינה
דפנה לויהאפשרות להירדם בהופעות וקונצרטים הולכת והופכת נוחה יותר. אבל אצל המוזיקאי הבריטי...
X 3 דקות
הדרך הנובעת מעצמה
דניאל אראלבלי אל שרוצה או משגיח, בלי מעשים שעלינו לעשות או לא לעשות,...
X 22 דקות